Инвестиции
Стартапам
Инвесторам
Инвесторам
Аналитика
Инвестиции
Стартапам
Инвесторам
Аналитика
Спрос и кооперация
Спрос и кооперация
Развитие и продвижение бизнеса
Спрос
Кооперация
Спрос и кооперация
Развитие и продвижение бизнеса
Спрос
Кооперация
Гранты и кредиты
Гранты и кредиты
Инфраструктура
Инфраструктура
Современные пространства
для бизнеса
для бизнеса
Инфраструктура
Современные пространства
для бизнеса
для бизнеса
Патентование
Патентование
Обучение и карьера
Обучение и карьера
Проекты для мегаполиса
Проекты для мегаполиса
Технологические городские проекты
Проекты для мегаполиса
О Кластере
О Кластере
Лидеры цифровой трансформации
Лидеры цифровой трансформации
Академия инноваторов
Академия инноваторов
Новатор Москвы
Новатор Москвы
Обучение и карьера
Обучение и карьера
Образовательные программы и база знаний
Обучение
Обучение и карьера
Образовательные программы и база знаний


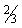 ×4×4 см, селезенки +3 см из-под края реберной дуги. В клиническом анализе
крови лейкоцитоз (14,2×109/л),
лимфоцитоз (56%), атипичные мононуклеары (12%), ускорена СОЭ (48 мм/час). ПЦР к ДНК ВЭБ в лимфоцитах крови положительна (+). Помимо стандартной
симптоматической терапии с первого дня лечения больному
был назначен Кипферон-суппозитории в суточной дозе - 1 млн ME ректально в два приема (через 12 часов), в течение 7 дней. Нормализация
температуры и уменьшение симптомов интоксикации отмечено на 2
сутки госпитализации. Ангинозный период закончен на 4 день госпитализации, к концу недели значительно улучшилось носовое дыхание. При
выписке отмечены нормальные размеры печени и селезенки,
значительно сократились лимфатические узлы шейных групп (в других группах не пальпируются). В клиническом анализе крови (с интервалом в 7 дней)
лейкоциты 6,2×109/л, лимфоциты
48%, моноциты 6%, СОЭ 22 мм/час, атипичных мононуклеаров нет.
×4×4 см, селезенки +3 см из-под края реберной дуги. В клиническом анализе
крови лейкоцитоз (14,2×109/л),
лимфоцитоз (56%), атипичные мононуклеары (12%), ускорена СОЭ (48 мм/час). ПЦР к ДНК ВЭБ в лимфоцитах крови положительна (+). Помимо стандартной
симптоматической терапии с первого дня лечения больному
был назначен Кипферон-суппозитории в суточной дозе - 1 млн ME ректально в два приема (через 12 часов), в течение 7 дней. Нормализация
температуры и уменьшение симптомов интоксикации отмечено на 2
сутки госпитализации. Ангинозный период закончен на 4 день госпитализации, к концу недели значительно улучшилось носовое дыхание. При
выписке отмечены нормальные размеры печени и селезенки,
значительно сократились лимфатические узлы шейных групп (в других группах не пальпируются). В клиническом анализе крови (с интервалом в 7 дней)
лейкоциты 6,2×109/л, лимфоциты
48%, моноциты 6%, СОЭ 22 мм/час, атипичных мононуклеаров нет.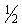 ×
5×5 см,
селезенки +4 см из-под края реберной дуги. Паренхиматозные органы были плотно-эластической консистенции, безболезненны при пальпации. В клиническом анализе крови лейкоцитоз (11,0×
109/л), лимфоцитоз (57%), атипичные мононуклеары (18%), ускорена СОЭ (24 мм/час). ПЦР к ДНК ВЭБ в лимфоцитах крови положительна. Помимо стандартной симптоматической терапии со второго дня
лечения
больному был назначен Кипферон-суппозитории в суточной дозе - 1 млн ME ректально в два приема (через 12 часов), в течение 7 дней. Нормализация температуры и уменьшение симптомов интоксикации
отмечено
на 2 сутки госпитализации. Ангинозный период закончен на 5 день госпитализации, к концу недели значительно улучшилось носовое дыхание. При выписке отмечены нормальные размеры селезенки,
значительно
сократились размеры печени (до
×
5×5 см,
селезенки +4 см из-под края реберной дуги. Паренхиматозные органы были плотно-эластической консистенции, безболезненны при пальпации. В клиническом анализе крови лейкоцитоз (11,0×
109/л), лимфоцитоз (57%), атипичные мононуклеары (18%), ускорена СОЭ (24 мм/час). ПЦР к ДНК ВЭБ в лимфоцитах крови положительна. Помимо стандартной симптоматической терапии со второго дня
лечения
больному был назначен Кипферон-суппозитории в суточной дозе - 1 млн ME ректально в два приема (через 12 часов), в течение 7 дней. Нормализация температуры и уменьшение симптомов интоксикации
отмечено
на 2 сутки госпитализации. Ангинозный период закончен на 5 день госпитализации, к концу недели значительно улучшилось носовое дыхание. При выписке отмечены нормальные размеры селезенки,
значительно
сократились размеры печени (до 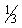 ×2×2 см) и шейных лимфатических узлов (в других группах
не
пальпируются). В клиническом анализе крови (с интервалом 9 дней) лейкоциты 7,2×109/л, лимфоциты 44%, моноциты 2%, атипичных мононуклеаров нет, СОЭ 5 мм/час.
×2×2 см) и шейных лимфатических узлов (в других группах
не
пальпируются). В клиническом анализе крови (с интервалом 9 дней) лейкоциты 7,2×109/л, лимфоциты 44%, моноциты 2%, атипичных мононуклеаров нет, СОЭ 5 мм/час.
