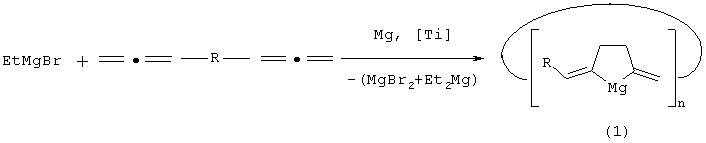Инвестиции
Стартапам
Инвесторам
Инвесторам
Аналитика
Инвестиции
Стартапам
Инвесторам
Аналитика
Спрос и кооперация
Спрос и кооперация
Развитие и продвижение бизнеса
Спрос
Кооперация
Спрос и кооперация
Развитие и продвижение бизнеса
Спрос
Кооперация
Гранты и кредиты
Гранты и кредиты
Инфраструктура
Инфраструктура
Современные пространства
для бизнеса
для бизнеса
Инфраструктура
Современные пространства
для бизнеса
для бизнеса
Патентование
Патентование
Обучение и карьера
Обучение и карьера
Проекты для мегаполиса
Проекты для мегаполиса
Технологические городские проекты
Проекты для мегаполиса
О Кластере
О Кластере
Лидеры цифровой трансформации
Лидеры цифровой трансформации
Академия инноваторов
Академия инноваторов
Новатор Москвы
Новатор Москвы
Обучение и карьера
Обучение и карьера
Образовательные программы и база знаний
Обучение
Обучение и карьера
Образовательные программы и база знаний


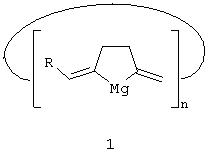 ,
, (1),
где
R=(СН2)4, (СН2)5, (СН2)6; n=3-5, заключающийся в том, что α,ω-диаллены общей формулы =•=-R-=•=, где
R=(CH2)4, (CH2)5, (СН2)6, подвергают взаимодействию с этилмагнийбромидом (EtMgBr) и магнием в порошке в мольном соотношении =•
=-R-=•=:EtMgBr:Mg, равном 10:(10-14):(5-7) в присутствии катализатора титанацендихлорида (Cp2TiCl2), взятого в количестве 0,3-0,7 ммолей по отношению к α,ω
-диаллену в ТГФ в атмосфере аргона при комнатной температуре (˜20°С) в течение 8-12 ч.
(1),
где
R=(СН2)4, (СН2)5, (СН2)6; n=3-5, заключающийся в том, что α,ω-диаллены общей формулы =•=-R-=•=, где
R=(CH2)4, (CH2)5, (СН2)6, подвергают взаимодействию с этилмагнийбромидом (EtMgBr) и магнием в порошке в мольном соотношении =•
=-R-=•=:EtMgBr:Mg, равном 10:(10-14):(5-7) в присутствии катализатора титанацендихлорида (Cp2TiCl2), взятого в количестве 0,3-0,7 ммолей по отношению к α,ω
-диаллену в ТГФ в атмосфере аргона при комнатной температуре (˜20°С) в течение 8-12 ч.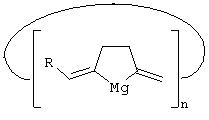 (1),
(1),