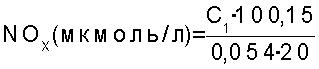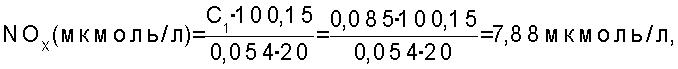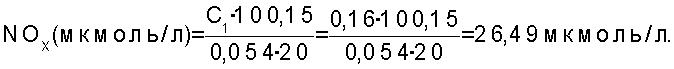Инвестиции
Стартапам
Инвесторам
Инвесторам
Аналитика
Инвестиции
Стартапам
Инвесторам
Аналитика
Спрос и кооперация
Спрос и кооперация
Развитие и продвижение бизнеса
Спрос
Кооперация
Спрос и кооперация
Развитие и продвижение бизнеса
Спрос
Кооперация
Гранты и кредиты
Гранты и кредиты
Инфраструктура
Инфраструктура
Современные пространства
для бизнеса
для бизнеса
Инфраструктура
Современные пространства
для бизнеса
для бизнеса
Патентование
Патентование
Обучение и карьера
Обучение и карьера
Проекты для мегаполиса
Проекты для мегаполиса
Технологические городские проекты
Проекты для мегаполиса
О Кластере
О Кластере
Лидеры цифровой трансформации
Лидеры цифровой трансформации
Академия инноваторов
Академия инноваторов
Новатор Москвы
Новатор Москвы
Обучение и карьера
Обучение и карьера
Образовательные программы и база знаний
Обучение
Обучение и карьера
Образовательные программы и база знаний


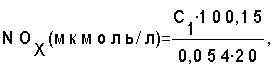 Изобретение относится к медицине, а именно к клинической биохимии, и касается способа определения нитратов и нитритов в слезной жидкости. Согласно
способу проводят осаждение белков 1,5 мл охлажденного до +4-8°С 96% этанола и 0,1 мл дистиллированной воды при конечной концентрации 86,4%, затем прибавляют 2 мл аммиачно-хлоридного буфера рН 9,
6±0,05 и дистиллированной водой доводят объем до 10 мл. Производят выделение нитратов и нитритов через кадмиевую колонку, проведение цветной реакции с добавлением
N-нафтилэтилендиаминдигидрохлорида, фотометрирование, определение концентрации нитратов и нитритов по графику зависимости концентрации от оптической плотности. Концентрацию нитратов и нитритов
определяют по формуле:
Изобретение относится к медицине, а именно к клинической биохимии, и касается способа определения нитратов и нитритов в слезной жидкости. Согласно
способу проводят осаждение белков 1,5 мл охлажденного до +4-8°С 96% этанола и 0,1 мл дистиллированной воды при конечной концентрации 86,4%, затем прибавляют 2 мл аммиачно-хлоридного буфера рН 9,
6±0,05 и дистиллированной водой доводят объем до 10 мл. Производят выделение нитратов и нитритов через кадмиевую колонку, проведение цветной реакции с добавлением
N-нафтилэтилендиаминдигидрохлорида, фотометрирование, определение концентрации нитратов и нитритов по графику зависимости концентрации от оптической плотности. Концентрацию нитратов и нитритов
определяют по формуле:
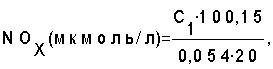
 где:
где: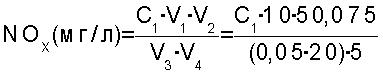
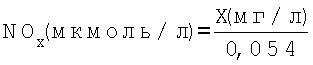 ,
где
,
где